在醫藥領域,制藥企業依靠藥品的專利保護的排他權獲得壟斷市場。隨著專利期限屆滿,仿制藥進入市場,原研藥廠依靠壟斷的銷售收入和利潤出現顯著的大幅下降。業內將這種現象其形象的比喻為“專利懸崖(Patent cliff )”。原研制藥企業當然不會坐以待斃,面對“專利懸崖”,其通過構建“基礎專利+次級專利”組合的方式,沿技術分支和產品開發時序進行布局,以累疊專利有效期,延長產品保護,拖延競爭對手的進入,維護壟斷利潤。我國制藥產業創新驅動不足,企業大多以仿制藥為主,對于國外制藥巨頭的布局策略,政府、企業都需要給予足夠的重視。
「引言」
制藥行業的研發具有投資大、風險高、周期長等特點,需要投入大量的金錢以及科研精力。如果沒有專利制度的保護,發明人將無法收回高昂的成本,從而喪失研發的動力。對于制藥行業中的企業來說,推出的新藥能否確保長期盈利和收入成為關切。在許多行業,一旦產品失去專利的排他權保護,企業一般都會面臨銷售額的大幅下降和利潤損失。在這一點,制藥行業表現的有為明顯,當專利權到期,隨著仿制藥廠商的進入,產品以較低的價格銷售,原研企業產品的原有的定價難以為繼。
業內將年銷售額大于10億美元的藥物稱為“重磅炸彈”(blockbuster),這些藥物一般占據公司收入的一大部分。歐盟的一項調查表明,仿制藥企業進入2年后,其報價僅為原研企業的40%。
「“專利懸崖”沖擊顯著且不可避免」
雖然專利藥到期后,有益于降低公眾的健康支出,提高社會福利,但是對于原研企業來說其不得不面對收入大幅下降的挑戰。失去排他限制后,這些產品將對公司的業績造成顯著的負面影響,還將迫使原研藥廠去尋找新的目標。醫藥企業價值鏈由研發驅動,對專利保護資產的依賴意味著制藥企業必須能夠不斷重復研發的成功。
這種高度依賴研發投入的商業模式,風險無處不在。制藥行業相較于其他行業具有獨特的研發特征,其屬于強研發驅動,高政策規則,產品復雜程度和質量要求越來越高。將一個“重磅炸彈”推出并得到市場的認可,一般花費超過10年時間,而專利的保護期限為20年。這種商業模式下,擁有“重磅炸彈”的制藥企業每經過10-12年左右的時間,就會面臨一次核心業務的調整。
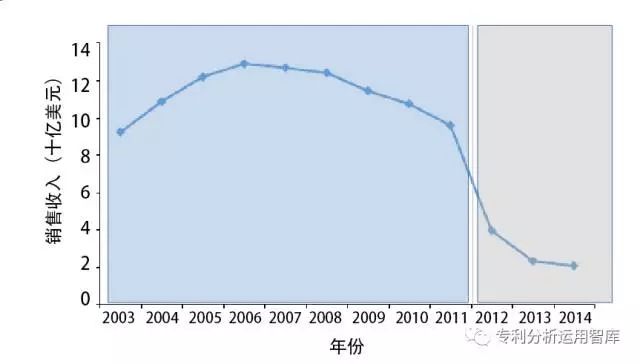
即將到來的“專利懸崖”對公司收入帶來巨大沖擊,導致公司財務上的巨大缺口。近年來,一些“重磅炸彈”藥物相繼失去專利保護。輝瑞公司的立普妥曾是非常暢銷的處方藥,隨著專利權2012年到期,其銷售情況隨之出現了大幅下降。
圖1.輝瑞公司產品立普妥lipitor?2003-2014年銷售收入(數據來源公司年報)
一般認為由專利保護到期給企業銷售收入下降不可避免,只能通過一些預防手段進行延緩。例如美國國會在Hatch-Waxman法案中規定了藥品專利期延長的制度。法案涉及美國新藥審批程序中的專利鏈接制度規定了適當延長藥品專利期限以彌補藥品因注冊審批期間而受到的經濟損失。
美國對藥品專利的延長可以有以下兩種途徑:一種是由美國專利商標局對于因專利審查延誤的專利給予保護時間的補償;另一種是針對因藥品行政許可審批程序而耽擱時間的,由美國專利商標局審核確認后給予補償,這種情況的補償期一般為5年,最多不超過14年,專利保護補償期從上市之日起計。
「造成“專利懸崖”的因素」
首先,原研制藥企業的“專利懸崖”現象主要由仿制藥企業的進入引起。仿制藥廠的進入給藥價帶來實質的影響,使得市場從壟斷轉向基于價格的競爭。仿制藥廠在研發上的投資遠遠低于原研藥廠,使其能夠將藥價定到一個較低的水平。競爭的引入打破了產品和價格的壟斷,造成原研企業銷量和售價的雙線調整,最終反應在銷售業績的快速下滑。
其次,近年來,原研企業研發產出持續下降。這一方面由于研發成本的增加,另一方面得歸因于政府對于藥品審批過程的延長,因此造成依賴研發驅動的制藥企業產品線的萎縮。
第三,仿制藥企業通過營銷手段影響醫務人員處方,來增加其市場占有率的行動更加積極,搶占了原研藥廠的市場份額。
第四,公共政策制定者為了控制成本維系公共健康體系穩定、可持續,往往傾向于處方相對便宜的仿制藥。
此外,隨著對于人類疾病分子水平的認知和藥物基因組學的研究導致個體化治療的出現。個體化的治療方案能夠提高臨床效果、增加病人的安全性,這些都是以往的“重磅炸彈”難以實現的。這種轉變也許將徹底重構藥物研發的結構和路徑。
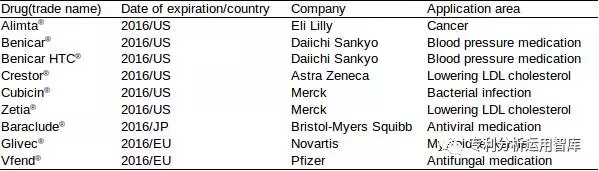
表1:2016年到期的重磅銷售藥物「數據來源于IMS (2012)」
對于研發驅動的制藥企業來說,如何確保現有產品線的收入,減緩仿制藥企業進入市場的沖擊變得日益重要,需要理性辯證的看待應對的策略。
「“專利懸崖”該如何應對」
總的來說,對于制藥企業而言其面對“專利懸崖”可選擇的策略大致可以分為四類:延長保護期進行防御、價格戰差異化競爭、妥協共享市場和創新開拓新產品線。該如何進行策略選擇,制藥廠商需要根據目前的能力、機會和優先考慮的選項等因素相機抉擇。
從四種策略的演進順序來講,首先應考慮如何延長專利的保護期,推遲“專利懸崖”的到來。本文將重點討論如何基于專利布局來進行策略性防御。
防御策略的一個基本原則是尋求延長市場排他權的可能性。策略導向是延長專利保護,取得暫時的保護或者干預競爭者的產品周期。主要手段是構建專利簇或專利組合,以基礎專利加次級專利的方式布局。基礎專利保護藥物活性組分及其制備,次級專利保護原始活性化合物的晶型、制劑、用途等,通過構建牢固的專利組合,以覆蓋藥物的各個方面。假設仿制藥廠挑戰基礎專利的有效性,次級專利的保護也將有助原研廠維持其市場份額。
對于基礎專利,化合物本身的保護也可考慮拆分成多個申請文件進行保護。例如,在一份申請中涵蓋多種化合物,同時在另一份申請中只包含特定的一個化合物。如果發現異構體取得了預料不到的技術效果,盡量考慮通過單獨的申請進行保護。藥物合成方法的改進的技術方案可以在后續的申請文件中予以保護,不必一開始就在化合物的申請文件中公開,可以選擇在產品周期的后續階段進行布局。對于次級專利,可以針對基礎專利技術方案的各種改進進行布局。
據統計,制藥企業在基礎專利到期日之前申請的次級專利與基礎專利的比例大概為7:1。這種申請顯然不是為了技術創新,而是為了將競爭對手排除在市場之外。因為對于仿制藥廠商來說,次級專利增加了判斷相關專利到期的難度,在進入相關市場時對于潛在的侵權行為有所顧忌。比如,仿制藥廠很可能會發現在已經明確化合物專利已經過期后,想要以一種更為經濟的方法生產該化合物或者使用其更為穩定的晶型時,又落入原研制藥企業次級專利的保護范圍內。
「舉個栗子-雅培HIV治療藥物的專利布局策略」
由雅培(abbvie)原研推上市場的治療HIV的藥物ritonavir通過外圍次級專利構建龐大的專利組合,在基礎專利到期后成功拖延了競爭對手的進入。雅培共圍繞lopinavir/ritonavir申請210件專利,將專利保護期至2028年,距基礎專利到期之日后12年之久。
技術分布方面:
在210件專利或申請中,涉及活性組分的化合物專利有2件,分別為US5,541,206涉及ritonavir,該專利申請于1995年,于2015年到期;及涉及lopinavir活性組分基礎專利US5,914,332于1996年申請,于2016年到期。
有81件(39%)相關專利涉及活性成分的組合物或制劑,活性組分的中間體,多晶型以及前藥。其中60%涉及組合物和制劑,27%覆蓋中間體,5%關于多晶型和無定型固體,另外有6件專利涉及前藥。多晶型對藥物的物理和藥代動力學特征有影響,例如,藥物的穩定性、溶解度、溶解速率、吸收和生物利用度等。
有68件(32%)相關專利涉及制備步驟和方法,包括制備與ritonavir、lopinavir類似結構的化合物、中間體以及制劑、組合物、多晶型的制備方法。
有31件(15%)相關專利針對HIV的制藥用途。專利涉及ritonavir、lopinavir在治療HIV感染或其他疾病的用途。其中US6,037,157(2016年到期)涉及改善ritonavir藥物被CYP3A4系統代謝的方法。
有28件(13%)屬于一般申請,這些專利申請涉及藥物組合物、制劑以及固體口服制劑的一般制備方法。這些申請雖未明確提及ritonavir、lopinavir但對與仿制藥廠來說仍是絆腳石。
專利時序方面:
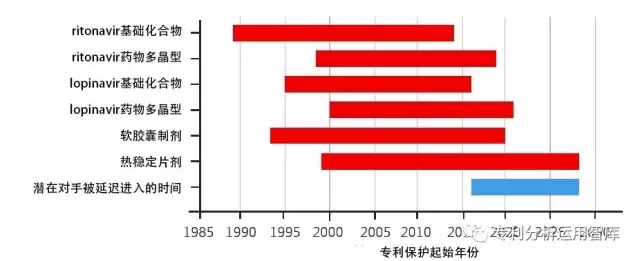
雅培選擇的后續專利申請多聚焦在多晶型、藥物用途和制劑,特別是熱穩定片劑。最終,在基礎化合物專利到期后,雅培覆蓋lopinavir、ritonavir的次級專利的保護期重疊至2028年,比基礎專利到期時限晚12年(參見圖2)。
其中,多晶型專利將ritonavir保護期延伸至2019年,將lopinavir保護期延伸至2021年。制劑相關申請涉及ritonavir、lopinavir/ritonavir的軟膠囊,其在時間上有重疊,這些專利最遲于2020年到期。
US7,346,752和US8,025,899專利均涉及lopinavir/ritonavir熱穩定片劑。這些專利涉及聚乙二醇及聚乙烯吡咯烷酮等水溶性聚合物輔料。類似的,專利申請US2007/0249692權利要求覆蓋了以上兩種聚合物輔料的組合。這些專利將在2025-2028年逐步到期。
而且這些專利組合保護范圍還涵蓋了對當前劑型的改進,雅培在保護新版的lopinavir、ritonavir藥物的同時,也豐富了產品線。如果上述專利被寫入橙皮書,這些不同的申請將能夠延遲仿制藥廠商的進入,從而延展當前市售制劑的專利保護期。
圖2.雅培lopinavir/ritonavir產品專利生命周期管理
(數據來自Health Affairs 31, no.10 :2286-2294)
「我國制行業相關政策的思考」
專利制度在賦予專利權人壟斷權的同時,也造成專利藥品高昂的價格。原研藥廠產品的保護的延長無疑會給依賴藥品的消費者帶來利益損害。這也體現了專利制度與公共健康權之間的矛盾。我國制藥企業以仿制藥廠商為主,國內企業與原研藥廠的競爭往往處于劣勢,在專利藥品領域遠低于全球平均水平。國內消費者面對高醫療費用的狀況短期內還難以緩解。
如何應對?
短期來說,發展中國家應對藥物多晶型及劑型改進的專利申請的創造性進行嚴格審查,對于顯而易見性的判斷標準應嚴格把握。在印度,如果請求保護對已知化合物的改進,則要求提供臨床效果作為技術方案具備創造性的依據。
同時還應對專利有效性進行積極挑戰,特別對于原研藥廠的次級專利。從雅培的策略可以看出,很多專利申請僅僅是對原始技術方案的微小改進,比如輔料的組合或選擇,國內制藥企業應積極對專利有效性進行挑戰或提交公眾意見。
長期而言,加快建立我國的橙皮書制度,增加原研藥廠專利透明度。而且不僅要列出直接相關授權專利,列出專利申請也十分必要。這對于亟待進入的仿制藥企業來說就能清楚的知道潛在的障礙。
此外,應建立對列入橙皮書專利的有效性進行審核。比如加拿大衛生部專利藥品和聯絡辦公室從第三方收集上市藥品的專利信息,其中包括對專利有效性等資質的核實,如果經辦公室審查發現該專利不應被列入,則會將該專利從列表中刪除。
「展望」
我國已是世界第一大原料藥生產和出口國、第二大OTC藥物市場、第三大醫藥市場,國內日益旺盛的需求完全可以成為國內醫藥行業發展的動力源泉。但從藥品銷售排名前列的品種看,國外一般都是專利藥,而國內基本是中藥注射劑以及專利過期的仿制藥。
國內制藥企業一方面需要持續進行技術改進,降低成本;另一方面則要加大投入開發高附加值的新產品。唯有依賴自主創新才能從根本上解決國內藥價貴,企業利潤低的悖論。